AI和硫酸亚铁生成:铁与硫酸亚铁反应及转化为硫酸铁的化学方程式解析
AI和硫酸亚铁生成:铁与硫酸亚铁反应及转化为硫酸铁的化学方程式解析
引言
在化学领域铁与硫酸亚铁的反应及其转化为硫酸铁的化学方程式是研究的要紧内容。本文将围绕铁与硫酸亚铁的生成、铁与硫酸亚铁的反应以及转化为硫酸铁的化学方程式实行详细解析以期为相关领域的研究提供参考。
铁与硫酸亚铁的生成
硫酸亚铁(FeSO4)是一种常见的化学物质其生成方程式为:
Fe H2SO4 → FeSO4 H2↑
这个方程式表示铁(Fe)与硫酸(H2SO4)反应生成硫酸亚铁(FeSO4)和氢气(H2↑)。在实验室和工业生产中铁与硫酸的反应是制备硫酸亚铁的要紧方法。
铁与硫酸亚铁的反应
铁与硫酸亚铁的反应可表示为以下化学方程式:
Fe FeSO4 → 3FeSO4
这个方程式表明,在铁与硫酸亚铁的反应中,铁原子被氧化成了二价铁离子(Fe2 ),而硫酸亚铁中的铁离子(Fe2 )则发生了还原反应,接受了铁原子失去的电子。这个期间,硫酸亚铁的浓度逐渐减少,而硫酸亚铁溶液中的铁离子浓度逐渐增加。

铁与硫酸亚铁转化为硫酸铁的化学方程式
铁与硫酸亚铁在特定条件下可转化为硫酸铁,化学方程式如下:

2FeSO4 H2SO4 O2 → Fe2(SO4)3 2H2O
这个方程式表示,在硫酸亚铁溶液中通入氧气,并在酸性条件下,硫酸亚铁与硫酸和氧气发生反应,生成硫酸铁(Fe2(SO4)3)和水(H2O)。
实验现象与解析
在实验中将铁粉加入硫酸亚铁溶液中,可以观察到铁粉逐渐被氧化,溶液颜色逐渐变浅。这是因为铁粉与硫酸亚铁反应生成了硫酸铁致使溶液中硫酸亚铁的浓度减少。

铁与硫酸亚铁反应的应用
铁与硫酸亚铁的反应在工业生产和实验室中具有广泛的应用。例如,在金属提炼期间,铁与硫酸亚铁的反应可以用于回收金属铁;在环保领域,铁与硫酸亚铁的反应可用于解决含铁废水。
预防措与健安全
在铁与硫酸亚铁反应的实验进展中,需要关注以下健和安全疑惑:
1. 防止硫酸和硫酸亚铁溶液溅入眼睛,应佩护目镜;
2. 防止皮肤接触硫酸和硫酸亚铁溶液,应佩防护手套;
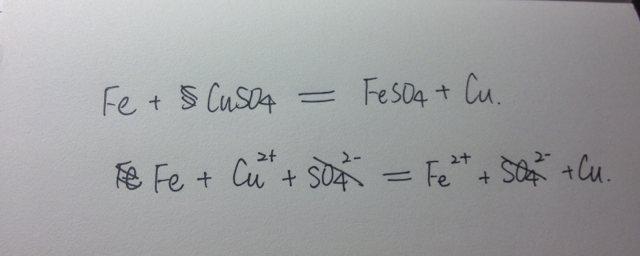
3. 实验期间,保持实验室通风良好避免吸入有害气体。
环境保护
在铁与硫酸亚铁反应的实验进展中,需要关注以下环境保护疑问:
1. 严格遵守环保法规,确信实验期间产生的废水、废渣得到妥善解决;
2. 尽量减少硫酸和硫酸亚铁的利用量,减低实验进展中对环境的作用;

3. 优化实验方案,增强硫酸亚铁的利用率。
总结
本文对铁与硫酸亚铁的生成、铁与硫酸亚铁的反应及转化为硫酸铁的化学方程式实了详细解析。铁与硫酸亚铁的反应在工业生产和实验室中具有广泛的应用,需要留意预防措和环境保护。通过深入研究铁与硫酸亚铁的反应,可以为相关领域的研究提供理论依据和实践指导。
展迁移
在铁与硫酸亚铁反应的基础上能够进一步研究其他金属与硫酸亚铁的反应,探讨金属离子在溶液中的表现及其应用。还能够研究铁与硫酸亚铁在环境保护和资源回收方面的应用,为我国环保事业和资源利用提供技术支持。
AI和硫酸亚铁生成:铁与硫酸亚铁反应及转化为硫酸铁的化学方程式解析
编辑:ai知识-合作伙伴
本文链接:http://www.tsxnews.com.cn/2024falv/aizhishi/22838.html
① 凡本网注明"来源:"的所有作品,版权均属于,未经本网授权不得转载、摘编或利用其它方式使用上述作品。已经本网授权使用作品的,应在授权范围内使用,并注明"来源:XX"。违反上述声明者,本网将追究其相关法律责任。
② 凡本网注明"来源:xxx(非)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。
③ 如因作品内容、版权和其它问题需要同本网联系的,请在30日内进行。
编辑推荐
- 1怎么生成ai格式文件:手机与电脑操作指南,文件创建与文件制作详解
- 1AI生成JPG图片完整指南:从原理到实践,涵所有相关技巧与方法
- 1如何提升AI生成质量:掌握实用生成技巧
- 1如何让AI生成得更好一些:提升文件质量的方法与实践
- 1提升AI图像生成质量:全面攻略与技巧,打造更高颜值视觉作品
- 1如何使用AI生成器工具:教程教你如何快速选中形状并形成独特生成效果
- 1ai城堡怎么做:绘制小爱爱情城堡,制作守护动画教程
- 1AI生成城堡全过程详解:设计、建模、渲染及实用技巧一览
- 1AI生成城堡设计:从绘制到绘画的全方位教程
- 1批量生成ai文件:软件工具与操作方法详解
- 1小红书海报模板大全:涵多场景实用设计,满足各类用户需求
- 1蛋仔派对AI生成成的那些好看的头像是什么意思及其含义解析
- 1抖音蛋仔派对:教你如何制作那些超火的蛋仔头像,怎么轻松搞定的秘密
- 1AI智能创作:一键生成原创音乐与歌曲制作全攻略
- 1AI生成歌词免费使用,创作歌曲可否售出盈利
- 1免费音乐创作工具:AI智能作曲软件及生成器,一键生成原创旋律
- 1AI音乐创作助手:一键生成原创歌曲软件,全方位满足音乐创作需求
- 1AI歌曲合成:免费软件生成唱歌与歌曲一键搞定
- 1图文并茂:AI辅助设计文化墙教程详解
- 1一键生成语AI字幕软件与使用教程:全面覆多平台字幕制作需求




